- rozwiązania
- 7 polubień
- 101846 odwiedzin

Spis treści:
1. Ocena zgodności, atestacja, oznaczenie CE2. Legalizacjaa) Jakie są typy legalizacji?b) Czym jest świadectwo legalizacji lub typ legalizacji?c) Co to jest przyrząd legalizowany?d) Kto wykonuje legalizacje przyrządów?e) Jakie typy przyrządów wymagają legalizacji?3. Wzorcowanie i kalibracjaa) Co to jest wzorcowanie, kalibracja?b) Co to jest świadectwo wzorcowania?c) Co to jest przyrząd wzorcowy?d) Czy wzorcowanie jest obowiązkowe? Kiedy trzeba wykonać wzorcowanie?e) Co to są punkty wzorcowania?f) Jakie laboratoria mogą przeprowadzać wzorcowanie i jakie wymagania muszą spełnić?g) Kiedy można wzorcować przyrządy w laboratorium nieakredytowanym? Kiedy wymagane jest wzorcowanie w laboratorium akredytowanym?h) Jaki jest okres ważności świadectwa wzorcowania?

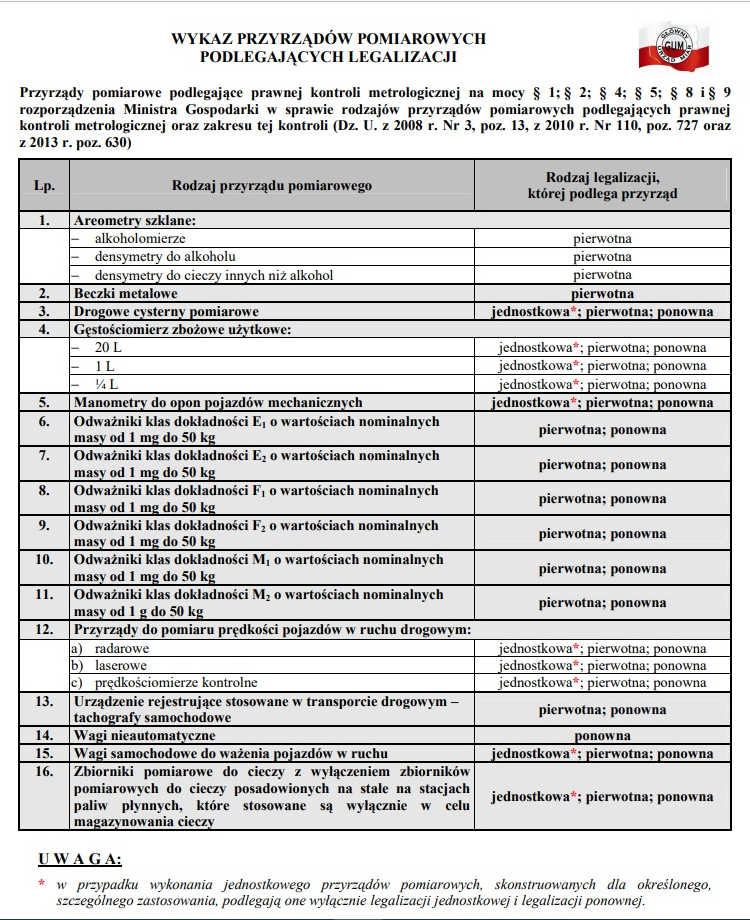
Świadectwo wzorcowania to dokument, który podaje odchylenie wskazań przyrządu wzorcowanego do wartości rzeczywistej (błąd pomiaru). Potocznie stosuje się także określenia świadectwo kalibracji, certyfikat kalibracji, certyfikat wzorcowania, świadectwo sprawdzenia. Świadectwo wzorcowania powinno być wystawione zgodnie z wzorem zalecanym przez Polskie Centrum Akredytacji (PCA) podanym ich na stronie internetowej.
Świadectwo wzorcowania powinno zawierać najważniejsze informacje takie jak: przedmiot wzorcowania, zgłaszającego, użytkownika, metodę wzorcowania, warunki środowiskowe, deklarację spójności pomiarowej oraz wyniki, które składają się z:
- wartości zmierzone,
- błędu pomiaru,
- niepewności pomiaru.
Przyrząd wzorcowy jest przyrząd, który został wywzorcowany i posiada świadectwo wzorcowania. Przykładowo wywzorcowany termometr wraz świadectwem wzorcowania można uznać się za termometr wzorcowy. Przyrząd wzorcowy musi posiadać rozdzielczość wskazań i dokładność pomiaru nie gorszą niż przyrządy, które będą przy jego pomocy sprawdzane.
Wzorcowanie powinno być przeprowadzane wszędzie tam, gdzie wykonywane pomiary mają wpływ na życie i zdrowie człowieka. W związku z tym wzorcowane powinny być przyrządy przeznaczone do:
- kontroli i monitorowania parametrów w lodówkach, zamrażarkach, cieplarkach, suszarkach, autoklawach, sterylizatorach, piecach, komorach klimatycznych,
- kontroli procesów i otoczenia w przemyśle spożywczym, farmaceutycznym i kosmetycznym,
- monitorowania temperatury i wilgotności w chłodniach, mroźniach, magazynach do przechowywania leków i żywności,
- monitorowanie temperatury w środkach transportu produktów spożywczych i farmaceutycznych.
Ponadto konieczność wzorcowania przyrządów określają niektóre normy, systemy zarządzania i przepisy prawne takie jak:
GMP (ang. Good Manufacturing Practice) – zbiór standardów bądź zasad związanych z Dobrą Praktyką Wytwarzania, stosowaną w szczególności w przemyśle farmaceutycznym, medycznym i spożywczym, opublikowany przez organizacje takie jak Food and drug Administration (FDA), Health Canada, World Health Organization (WHO) i inne, np.
- Regulacja FDA 21 CFR część 820 - Good Manufacturing Practice for medical devices, podrozdział D, sekcja 820.61 – Measurement equipment
Cyt: "All production and quality assurance measurement equipment, such as mechanical, automated, or electronic equipment, shall be suitable for its intended purposes and shall be capable of producing valid results. Such equipment shall be routinely calibrated, inspected, and checked according to written procedures."
Tłumaczenie własne: "Całe wyposażenie pomiarowe stosowane do kontroli produkcji oraz zapewnienia jakości, w tym wyposażenie mechaniczne, wyposażenie do automatyzacji oraz wyposażenie elektroniczne, powinno być odpowiednie do zamierzonych celów i pozwalać na uzyskiwanie właściwych wyników. Takie wyposażenie powinno być rutynowo wzorcowane i sprawdzane zgodnie z ustalonymi procedurami."

- WHO 40-sty Raport Techniczny, aneks 4 - Supplementary guidelines on Good Manufacturing Practices: validatio
Cyt: "7.1 Calibration and verification of equipment, instruments and other devices, as applicable, used in production and quality control should be performed at regular intervals."
Tłumaczenie własne: "Wzorcowanie i sprawdzanie wyposażenia, przyrządów pomiarowych i innych urządzeń stosowanych w produkcji i kontroli jakości powinno być przeprowadzane w regularnych odstępach czasu."
- Rozporządzenie Ministra Zdrowia z dnia 1.10.2008 r. w sprawie wymagań Dobrej Praktyki Wytwarzania (Dz. U. 2008 nr 184 poz. 1143, z późn. zm.)
Cyt: "5.3 Kalibracja
5.30 Wyposażenie do kontroli, ważenia, mierzenia, monitorowania i testowania, krytyczne dla jakości produktów pośrednich i farmaceutycznych substancji czynnych, powinno być kalibrowane zgodnie z pisemnymi procedurami i ustalonym harmonogramem."
GLP (ang. Good Laboratory Practice) – zbiór standardów bądź zasad związanych z Dobrą Praktyką Laboratoryjną, opublikowany przez organizacje takie jak Food and drug Administration (FDA), World Health Organization (WHO) i inne, np.
- Regulacja FDA 21 CFR część 58 - Good Laboratory Practice for nonclinical laboratory studies, podrozdział D, sekcja 58.63 – Maintenance and calibration of equipment
Cyt: "Equipment used for the generation, measurement, or assessment of data shall be adequately tested, calibrated and/or standardized."
Tłumaczenie własne: "Wyposażenie stosowane do generowania, mierzenia lub oceny danych powinno być odpowiednio testowane, wzorcowane i/lub standaryzowane."
- Rozporządzenie Ministra Zdrowia z dnia 4 czerwca 2003 r. (Dz.U. 2003 nr 116 poz. 1103 ) w sprawie kryteriów, które powinny spełniać jednostki organizacyjne wykonujące badania substancji i preparatów chemicznych, oraz kontroli spełnienia tych kryteriów (odnoszące się do bezpośrednio do zasad Dobrej Praktyki Laboratoryjnej – GLP).
Cyt: "Jednostka badawcza zapewnia, że: 2) przyrządy pomiarowe stosowane do badań są okresowo sprawdzane, czyszczone, konserwowane i wzorcowane, zgodnie ze Standardowymi Procedurami Roboczymi, i czynności te są każdorazowo odnotowane."
GDP (ang. Good Distribution Practice) – zbiór standardów bądź zasad związanych z Dobrą Praktyką Dystrybucyjną, np.
- Wytyczne z dnia 7 marca 2013r. w sprawie Dobrej Praktyki Dystrybucyjnej dotyczącej produktów leczniczych do stosowania u ludzi, odnoszące się do 3 dyrektywy 2001/83/WE
Cyt: "3.3. Sprzęt używany do kontrolowania lub monitorowania otoczenia, w którym przechowywane są produkty lecznicze, powinien być kalibrowany w określonych odstępach czasu w oparciu o ocenę ryzyka i niezawodności."
ISO 22000
Cyt: "... do zapewnienia ważnych wyników, wyposażenie pomiarowe i metody używane a) powinny być kalibrowane i weryfikowane w zaplanowanych odstępach czasu..."
ISO 9001
Cyt: "7.6 Tam, gdzie niezbędne jest zapewnienie wiarygodnych wyników, wyposażenie pomiarowe należy wzorcować i/lub sprawdzać w ustalonych odstępach czasu lub przed użyciem w odniesieniu do wzorców jednostek miary powiązanych z międzynarodowymi lub państwowymi wzorcami jednostek miary."
ISO 17025
Cyt: "5.6.1. Całe wyposażenie używane do badań i/lub wzorcowań, w tym wyposażenie do pomiarów pomocniczych (np. warunków środowiskowych), które ma znaczący wpływ na dokładność lub miarodajność wyników badania, wzorcowania lub pobierania próbki powinno być wzorcowane przed oddaniem do użytkowania."
ISO 22716 (zawierająca zasady Good Manufacturing Practice powołane w Rozporządzeniu Parlamentu Europejskiego i Rady (WE) nr 1223/2009/WE z dnia 30.11.2009r. dotyczące produktów kosmetycznych.
Cyt: "5.4.1 Laboratory and production measuring instruments that are important for the quality of the product, should be calibrated regularly."
Tłumaczenie własne: "Przyrządy pomiarowe stosowane w laboratorium bądź w produkcji, które mają istotny wpływ na jakość produktu powinny być regularnie wzorcowane."
- Rozporządzenie Parlamentu Europejskiego i Rady (WE) nr 1223/2009/WE z dnia 30.11.2009 roku, dotyczące produktów kosmetycznych, które narzuca na producentów wyrobów kosmetycznych obowiązek produkcji kosmetyków zgodnie z Dobrymi Praktykami Produkcyjnymi (GMP), Artykuł 8, Dobra praktyka produkcji
Cyt: "1. Aby zapewnić realizację celów art.1, produkcja produktów kosmetycznych odbywa się zgodnie z dobrą praktyką produkcji."

Wzorcowanie jak już wcześniej zdefiniowano wykonuje się w ustalonych warunkach lub inaczej w określonych punktach wzorcowania. Punkty wzorcowania są to konkretne wartości parametru mierzonego przez dany przyrząd, w których przyrząd ma być wzorcowany. Przykładowo dla termometru lub rejestratora temperatury punktami wzorcowania będą konkretne wartości temperatury, w których ten termometr lub rejestrator będzie wzorcowany. W tabeli poniżej przedstawione zostały przykładowe zakresy temperatur dla przechowywania żywości i leków.
| Produkt | Przedział temperatur |
| mięso świeże, chłodzone, z wyjątkiem mięsa drobnego, mielonego i podrobów | -1°C do +7°C |
| podroby, mięso drobne i mielone, chłodzone | -1°C do +3°C |
| mięso i podroby mrożone | <-12°C |
| mięso i podroby głęboko mrożone | <-18°C |
| leki | W zależności od typu produktu najczęściej są to przedziały: +2°C do +8°C +8°C do +15°C +15°C do +25°C |
W przypadku pierwszego zestawu punktów wzorcowania temperatury (-1°C, +3°C, +7°C) termometr można w sposób udokumentowany świadectwem wzorcowania zastosować tylko do kontroli temperatury mięsa chłodzonego. Przy wyborze punktów wzorcowania z zestawu drugiego (-25°C, +0°C, +25°C) termometr można zastosować nie tylko do kontroli temperatury mięsa chłodzonego, ale także do kontroli temperatury mięsa mrożonego.
Na przykładzie danych z powyższej tabelki wynika, że termometr stosowany do kontroli temperatury mięsa chłodzonego powinien być wzorcowany co najmniej w zakresie od -1°C do +7°C. W tym przypadku punkty wzorcowania mogą być następujące: -1°C, +3°C, +7°C, albo także -25°C, +0°C, +25°C.Zgodnie z dobrą praktyką metrologiczną przyrządy powinny być wzorcowane w minimum 3 punktach. Wzorcowanie tylko w jednym punkcie jest uzasadnione wtedy, gdy dla użytkownika krytyczna jest tylko jedna konkretna wartość parametru. Punkty wzorcowania powinny być tak dobrane przez klienta zamawiającego usługę wzorcowania, aby pokrywały cały wykorzystywany zakres pomiaru mierzonej wielkości.
Ze względu na to, że zakres pomiaru temperatur od -25°C do +25°C jest jednym z najczęściej wykorzystywanych zakresów temperatur przez użytkowników przyrządów, Laboratorium Wzorcujące firmy MERA ustaliło, że punkty temperatury -25°C, 0°C, +25°C są tzw. "punktami standardowymi temperatury". Punkty standardowe laboratorium są punktami, które domyślnie są proponowane tym klientom, którzy nie mają ściśle określonych wymagań, co do punktów wzorcowania przyrządów.


Wzorcowanie przyrządów pomiarowych mogą przeprowadzać: krajowe instytucje metrologiczne (Główny Urząd Miar) Instytuty Desygnowane będące depozytariuszami wzorców państwowych oraz laboratoria akredytowane i laboratoria nieakredytowane. Laboratoria nieakredytowane oraz laboratoria akredytowane muszą spełniać wymagania Polskiego Centrum Akredytacji (PCA) podane w dokumencie DA-06 dotyczące zapewnienia spójności pomiarowej, polegające na okresowym wzorcowaniu stosowanego w tych laboratoriach wyposażenia pomiarowego przez odpowiednie organizacje (punkt 4.1.):
"Wyposażenie pomiarowe (np. przyrządy pomiarowe, wzorce pomiarowe, układy pomiarowe, wyposażenie badawcze spełniające funkcje pomiarowe) stosowane do wzorcowań/kalibracji, pomiarów, badań i inspekcji, mające istotny wpływ na niepewność pomiaru związaną z wynikami tych działań powinno być wzorcowane przez krajowe instytucje metrologiczne – NMI (w Polsce funkcję NMI pełni Główny Urząd Miar (GUM)), albo Instytuty Desygnowane – DI (Designated Institutes) będące depozytariuszami wzorców państwowych, będące sygnatariuszami porozumienia CIPM MRA, albo przez laboratoria akredytowane przez sygnatariuszy porozumień EA MLA lub ILAC MRA ".
W związku z tym wymaganiem klienci mają prawo żądać od laboratoriów nieakredytowanych dokumentu potwierdzającego zapewnienie spójności pomiarowej czyli świadectw wzorcowania wyposażenia pomiarowego stosowanego w tych laboratoriach. W laboratoriach akredytowanych dowodem, potwierdzającym spełnienie tych wymagań jest znak akredytacji.
Laboratoria akredytowane muszą spełniać także wymagania normy dotyczącej akredytacji laboratoriów wzorcujących ISO 17025 oraz zakończyć z wynikiem pozytywnym audyt prowadzony przez jednostkę akredytującą laboratoria wzorcujące (w Polsce PCA), weryfikujący spełnienie wymagań tej normy. Ponadto, aby utrzymać akredytację w laboratorium akredytowanym konieczne jest pozytywne przejście okresowych corocznych audytów kontrolnych.
Stanowisko dotyczące wzorcowań w laboratoriach nieakredytowanych i akredytowanych znajdują się także w oficjalnej odpowiedzi Polskiego Centrum Akredytacji na pismo wystosowane przez firmę MERA z prośbą o udzielenie wyjaśnień w tej sprawie (załącznik nr 1).

Generalnie większość przepisów i norm nie narzuca wykonywania wzorcowania w laboratorium akredytowanym. Stanowisko dotyczące wzorcowań w laboratoriach nieakredytowanych i akredytowanych znajdują się także w oficjalnej odpowiedzi Polskiego Centrum Akredytacji na pismo wystosowane przez firmę MERA z prośbą o udzielenie wyjaśnień w tej sprawie (załącznik nr 1). Ponadto wzorcowanie w laboratorium akredytowanym jest zalecane w oparciu o normę ISO/TS 16949. Zgodnie z wymaganiami pozostałych norm i przepisów wystarczające jest wykonanie wzorcowania w laboratorium nieakredytowanym.
Zgodnie z zalecanym przez Polskiego Centrum Akredytacji (PCA) wzorem świadectwa wzorcowania na świadectwach wzorcowania standardowo nie podaje się daty ważności. Urządzenia pomiarowe wraz z biegiem czasu przyrządy się rozkalibrowują i po pewnym okresie nie nadają się do użytkowania. W związku z tym jednorazowe wykonanie wzorcowania, np. przy zakupie przyrządu nie jest wystarczające. Zgodnie z odpowiednimi normami, rozporządzeniami i innymi przepisami prawnymi wzorcowanie należy cyklicznie powtarzać w całym okresie użytkowania przyrządu:
- ISO 9001
Cyt: "7.6 Tam, gdzie niezbędne jest zapewnienie wiarygodnych wyników, wyposażenie pomiarowe należy wzorcować i/lub sprawdzać w ustalonych odstępach czasu lub przed użyciem w odniesieniu do wzorców jednostek miary powiązanych z międzynarodowymi lub państwowymi wzorcami jednostek miary."


- ISO 22000
Cyt: "... do zapewnienia ważnych wyników, wyposażenie pomiarowe i metody używane
a) powinny być kalibrowane i weryfikowane w zaplanowanych odstępach czasu..." - Rozporządzenie Ministra Zdrowia z dnia 1.10.2008 r. w sprawie wymagań Dobrej Praktyki Wytwarzania (Dz. U. 2008 nr 184 poz. 1143, z późn. zm.)
Cyt: "5.3 Kalibracja
5.30 Wyposażenie do kontroli, ważenia, mierzenia, monitorowania i testowania, krytyczne dla jakości produktów pośrednich i farmaceutycznych substancji czynnych, powinno być kalibrowane zgodnie z pisemnymi procedurami i ustalonym harmonogramem." - Rozporządzenie Ministra Zdrowia z dnia 4 czerwca 2003 r. (Dz.U. 2003 nr 116 poz. 1103 ) w sprawie kryteriów, które powinny spełniać jednostki organizacyjne wykonujące badania substancji i preparatów chemicznych, oraz kontroli spełnienia tych kryteriów (odnoszące się do bezpośrednio do zasad Dobrej Praktyki Laboratoryjnej – GLP).
Cyt: "Jednostka badawcza zapewnia, że:
2) przyrządy pomiarowe stosowane do badań są okresowo sprawdzane, czyszczone, konserwowane i wzorcowane, zgodnie ze Standardowymi Procedurami Roboczymi, i czynności te są każdorazowo odnotowane." - Wytyczne z dnia 7 marca 2013r. w sprawie Dobrej Praktyki Dystrybucyjnej dotyczącej produktów leczniczych do stosowania u ludzi, odnoszące się do 3 dyrektywy 2001/83/WE
Cyt: "3.3. Sprzęt używany do kontrolowania lub monitorowania otoczenia, w którym przechowywane są produkty lecznicze, powinien być kalibrowany w określonych odstępach czasu w oparciu o ocenę ryzyka i niezawodności."
Dokumenty prawne i normy nie narzucają okresów w jakich należy ponawiać wykonanie wzorcowania. Terminy ponownych wzorcowań powinien ustalić użytkownik na podstawie własnych obserwacji, zaleceń producenta przyrządu lub dostępnych wytycznych,np. w dokumencie "ILAC-G24:2007/ OIML D 10:2007 (E), Wytyczne dotyczące wyznaczania odstępów czasu między wzorcowniami przyrządów pomiarowych (tłumaczenie Polskie Centrum Akredytacji, 24.08.2010r.)" dostępne pod linkiem: Wytyczne wyznaczania odstępów czasu między wzorcowaniami Okres ponownego wzorcowania przyrządu wybiera się zazwyczaj z okresu czasu od 6 miesięcy do 2 lat, a do czynników, które należy uwzględnić do określenia terminu ponownego wzorcowania należą:
- jak bardzo istotny jest pomiar wykonywany przyrządem wzorcowanym
Przykład nr 1. Pomiar wykonywany przyrządami do kontroli temperatury przechowywania leków bądź żywności ma bardzo ważny wpływ na życie i zdrowie ludzi i dlatego przyrządy te powinny być wzorcowane w stosunkowo krótkich odstępach czasu, zalecane jest wzorcowanie minimum raz do roku.
Przykład nr 2. Pomiar przyrządami do kontroli warunków w pomieszczeniu biurowym nie jest bardzo istotny i mogą być one wzorcowane np. raz na 2 lata. - koszty spowodowane zastosowaniem zużytego przyrządu
Przykład nr 1. Przyrządy stosowane do kontroli temperatury przechowywania w magazynie drogich leków powinny być często wzorcowane, gdyż zastosowanie zużytego przyrządu (przyrządu rozregulowanego wskutek użytkowania w dłuższym okresie czasu i nie poddanego wzorcowaniu w stosownym terminie) może spowodować konieczność wycofania z dalszej sprzedaży i zutylizowania całej partii leków. Wzorcowanie zalecane minimum raz do roku.
Przykład nr 2. Zastosowanie rozregulowanego przyrządu do monitorowania warunków w pomieszczeniu biurowym nie wywoła konieczności poniesienia wysokich kosztów.


- warunki pracy przyrządu
Przykład nr 1. Przyrządy są wykorzystywane w ciężkich warunkach takich jak np. silne zapylenie, skrajne warunki temperatury pracy przyrządu, itp. wówczas przyrządy powinny być często wzorcowane, np. co 6 lub co 9 miesięcy.
Przykład nr 2. Przyrządy są użytkowane w lekkich warunkach, wówczas wzorcowanie przyrządów można przeprowadzać co 2 lata. - częstotliwość użytkowania
Przykład nr 1. Przyrządy są użytkowane intensywnie, wówczas wzorcowanie powinno być wykonywane raz do roku.
Przykład nr 2. Przyrządy są użytkowane nieregularnie bądź rzadko, wówczas wzorcować można je raz na 2 lata.
Dla uproszczenia powszechnie przyjmuje się konieczność wykonywania przyrządów raz do roku i taki termin ponownego wzorcowania jest zalecany przez laboratorium wzorcujące firmy MERA. Ponadto w przypadkach, gdy jednocześnie występuje kilka czynników krytycznych, np. przyrząd jest intensywnie użytkowany w trudnych warunkach przy dużym zapyleniu i wysokiej temperaturze otoczenia, to wówczas należy rozważyć zwiększenie częstotliwości wzorcowań, zalecane raz na 6 miesięcy.
Co więcej użytkownik przyrządu powinien także w krótkich odstępach czasu dokonywać we własnym zakresie sprawdzeń przyrządu w celu możliwie szybkiego wykrycia potencjalnego zużycia bądź rozregulowania przyrządu i wyłączenia go z użytkowania. Sprawdzenia można dokonać poprzez porównanie wskazań z innym wywzorcowanym przyrządem w warunkach, w których jest stosowany, np. w lodówce.
W przypadku wykrycia w wyniku takiego porównania przekroczenia przez dany przyrząd błędu dopuszczalnego zalecane jest przesłanie przyrządu do laboratorium wzorcującego celem weryfikacji bądź ponownego wzorcowania. Jeśli laboratorium potwierdzi zużycie bądź rozregulowanie przyrządu to użytkownik powinien zaopatrzyć się w nowy przyrząd wraz ze świadectwem wzorcowania.
Chętnie odpowiem na Państwa pytania i pomogę dobrać optymalne rozwiązanie spełniające Państwa potrzeby!

tel. +22 535 16 69











